Roztroušená skleróza mozkomíšní – co by měl nelékař vědět?
"Roztroušená skleróza je chronické onemocnění postihující centrální nervový systém. Neléčené onemocnění způsobuje v průběhu 10–20 let závažnou invaliditu u většiny pacientů. Díky včas nasazené moderní léčbě je možno průběh nemoci u velké části pacientů podstatně ovlivnit. Nemoc zasahuje do různých oblastí života pacienta a správná pomoc tedy vyžaduje spolupráci nejen lékařů, ale celé řady dalších odborníků," píše na úvod svého článku lékařka Dana Horáková z Neurologické kliniky 1. LF UK a VFN v Praze.
obsah
- Co je roztroušená skleróza (RS)
Jak nemoc vzniká
Jaké jsou potíže při RS
Co nemoc způsobuje
Jak se určuje diagnóza RS
Jaký má nemoc průběh
Jaké jsou možnosti léčby
Jak může pacient sám ovlivnit průběh choroby
RS a těhotenství
RS a dědičnost
Omezení pacienta s RS
Závěr
Literatura
Co je roztroušená skleróza (RS)
Odpověď na tuto otázku není jednoduchá. Pod nálepkou RS se totiž skrývá velké množství rozdílných typů a stupňů postižení, která mohou pacientovi různě komplikovat život, a to od relativně lehkých až po těžká, rychle probíhající postižení. V současnosti mluvíme o RS jako o jednom onemocnění, je ale pravděpodobné, že se v budoucnu RS rozpadne na více podjednotek, které budou lépe charakterizovat jednotlivé skupiny pacientů (Weiner 2009).
Jak nemoc vzniká
Co v současnosti o nemoci víme? Nemoc postihuje především mladé osoby, nejčastější začátek je mezi 20–30 rokem života a častěji jsou postiženy ženy (2–3x častěji). Základem klinických obtíží je zánětlivé postižení centrálního nervového systému, tj. mozku a míchy. Při slově zánět si většina laiků představí infekci, tedy bakterie nebo viry, které napadají určitou tkáň. Kromě infekčního zánětu ale existují i jiné typy zánětu, např. zánět autoimunitní.
To je právě případ RS. Jeho podstatou je určitá porucha v imunitním systému (IS) člověka, velmi zjednodušeně řečeno IS se jakoby „zblázní“ a začne dělat to, co dělat nemá. Jeho základní funkcí je totiž chránit člověka před infekcemi a tělu cizími strukturami (např. nádorovými nebo odumřelými buňkami). K tomu je IS velmi dobře vychován a jeho buňky umí dobře rozpoznávat vlastní, zdravé buňky, kterých si nevšímají, a buňky cizí, které většinou rychle zlikvidují.
V případě autoimunitních nemocí je právě problém v tom, že se IS splete a začne napadat vlastní tkáně. Autoimunitních nemocí je celá řada, např. lupénka (IS napadá kožní buňky), revmatoidní artritida (jsou napadány kloubní struktury), Crohnova nemoc s poškozením střeva nebo RS. Zde jsou cílem útoku struktury mozku a míchy.
Jaké jsou potíže při RS
Podle toho, kde zánět aktuálně vzplane, může mít pacient různé klinické obtíže. Nejčastěji se jedná o poruchy citlivosti (stěhovavé necitlivosti, brnění, bolesti), poruchy hybnosti (obrny končetin) či zraku (typickým projevem je jednostranná porucha, jakoby vidění přes igelit nebo špinavé sklo, často doprovázená bolestí oka při pohybu). Může být ale i porucha stability, závratě, dvojité vidění, poruchy svěračů či nálady (nejčastěji deprese).
Co nemoc způsobuje
Proč k poruše v imunitním systému dojde, není dnes ještě zcela přesně známo, téměř jistě ale víme, že jedním z faktorů je vrozená dispozice (Oksenberg, Barazini et al. 2008). Tedy pacient se již narodí s určitou poruchou ve svých genech, které řídí činnost IS a tyto geny dávají buňkám IS špatné signály.
Určitě dnes víme, že se nejedná o jeden gen, nýbrž o skupinu genů (polygenní onemocnění). Zřejmě kombinace dobrých a špatných genů je do určité míry odpovědná za tíži postižení. Samotné geny ale nestačí. Obdobnou dispozici mají totiž statisíce lidí v populaci, a přesto nemoc nikdy nedostanou. Vrozená dispozice se tedy musí ještě v průběhu života s něčím setkat.
Z vnějších faktorů, které spustí tuto připravenou dispozici, jsou nejvíce podezírány různé virové infekce (zejména skupina herpetických virů způsobující např. infekční mononukleózu nebo opary), dále kouření a nedostatek vitaminu D. Role vitaminu D je velmi zajímavá. Tento vitamin se vytváří vlivem slunečního záření v kůži a tedy je logické, že jeho hladina bude podstatně vyšší u lidí žijících blíže k rovníku. Tomu odpovídá i výskyt RS, kdy skutečně nejnižší výskyt je kolem rovníku a směrem od rovníku na sever a na jih se počty pacientů významně zvyšují. Pravděpodobně kritické je již období vývoje plodu v děloze, kdy vitamin D má důležitou úlohu právě ve správné výchově buněk imunitního systému. Pokud ho má matka nedostatek, tak už v tomto období se může IS plodu vyvíjet nesprávně (Ramagopalan, Maugeri et al. 2009). Neznamená to ale, že by měly těhotné ženy masivně nadužívat vitamin D. Tímto vitamínem je totiž možné se i předávkovat a doporučenou dávku je nutno konzultovat s lékařem.
Přesné poznání faktorů způsobujících RS a vztahů mezi nimi je v současnosti cílem velmi intenzivního výzkumu. Pokud se nám v budoucnu podaří lépe rozpoznat např. jednotlivé geny, které jsou odpovědné za tíži nemoci, tak budeme moci již na počátku nemoci daleko lépe určit prognózu konkrétních pacientů. Tady nás ale čeká ještě velký kus práce.
Jak se určuje diagnóza RS
Nyní tedy víme, co nemoc pravděpodobně způsobuje a jak se může projevovat. Dalším logickým krokem je zjistit, zda při daných obtížích, které vypadají jako RS, pacient skutečně RS má. Základem určení diagnózy je kombinace klinického vyšetření s podrobným vyhodnocením historie pacienta (anamnézy) a pomocných metod. Z těch jsou dnes suverénně na 1. místě magnetická rezonance a vyšetření mozkomíšního moku.
Magnetická rezonance (MR) je vyšetření velmi citlivé, které nám podrobně ukáže strukturu mozku a míchy. Pro RS typická jsou zánětlivá ložiska vypadající jako bílé fleky v nervové tkáni (Montalban, Tintore et al. 2010). Ne každý bílý flek ale znamená RS, vždy je nutno brát v úvahu celou řadu faktorů, jako je věk pacienta, předchozí onemocnění a zejména další vývoj nálezu. Někdy jsme schopni již po 1. vyšetření říci s velkou pravděpodobností, že se o RS jedná. Jindy teprve čas přinese definitivní rozhodnutí. Typické pro RS je objevování se a mizení ložisek na kontrolních rezonancích.
Magnetická rezonance má dnes zásadní význam pro diagnostiku nemoci, stále více se ale používá i pro sledování aktivity nemoci. Vyšetření je velmi bezpečné, nelze ho provést pouze u pacientů s kovovými předměty v těle (zejména kardiostimulátor a jiné implantáty). Dále je třeba speciální režim u osob trpících klaustrofobií (strach z uzavřených prostor). To nelze nikdy podcenit a své obavy je nutné vždy dopředu probrat s lékařem.
Druhým vyšetřením je rozbor mozkomíšního moku (likvoru). Ten získáváme prostřednictvím lumbální punkce, což je za standardně provedených podmínek relativně jednoduché vyšetření, které je často pacienty zbytečně démonizováno. Punkci, pokud lze, provádíme vsedě. Je to totiž technicky podstatně jednodušší. Mok odebíráme lumbální jehlou z kanálu páteřního, nikoli z míchy! Vlastní vyšetření je samozřejmě vpich, pokud ale vše proběhne tak, jak má být, tak celý zákrok netrvá déle než 10 minut.
Nejčastější komplikací výkonu je kolaps pacienta. Ten je způsoben většinou poklesem krevního tlaku v důsledku přirozeného strachu pacienta. Vždy je třeba udělat maximum pro pacientův komfort, výkon mu řádně vysvětlit a pokusit se ho zbavit nepřiměřeného strachu. Nejčastější komplikací po punkci je tzv. postpunkční bolest hlavy, která se objevuje většinou druhý až třetí den a představuje dosti intenzivní bolest po postavení. Její příčinou je otvor, který může zůstat ve tkáních, kudy procházela lumbální jehla. Tímto otvorem může potom unikat mozkomíšní mok, což vede k poklesu tlaku v likvorových cestách. Komplikace je většinou nezávažná, vyžaduje několikadenní klid, dostatek tekutin a případně běžné léky na bolest. Hlavní prevencí této komplikace je užívání tzv. atraumatické lumbální jehly, která je speciálně vyrobena tak, aby minimálně poškodila pleny.
Skutečně dle vlastních zkušeností můžeme potvrdit, že s těmito jehlami se výskyt postpunkčních bolestí hlavy podstatně snížil. Získaný mozkomíšní mok se odesílá na celou řadu vyšetření, která potvrdí nebo vyloučí zánětlivý proces. Důležité je i to, že nám vyšetření likvoru může napomoci ve vyloučení dalších onemocnění, jako jsou např. některé infekce (borelioza, aktivní herpetické infekce).
Po vyhodnocení výsledků obou těchto základních vyšetření již můžeme u velké části pacientů s velkou jistotou říci, zda se o RS jedná či nikoli. Samozřejmě jsou i případy, které jsou podstatně složitější a vyžadují další sledování a vyšetření, popis všech těchto diferenciálně diagnostických možností ale již přesahuje rámec našeho článku.
Jaký má nemoc průběh
Co tedy můžeme pacientovi, u kterého jsme právě potvrdili roztroušenou sklerózu, říci? Co může od nemoci očekávat?
Nejčastější průběh nemoci je tzv. relaps remitentní forma (80–85 % pacientů, viz obr. 1). Znamená to, že se u pacienta střídají období klinických obtíží = ataky (relapsy), s obdobími klinické stabilizace = remise. První ataku nazýváme klinicky izolovaný syndrom (CIS). Teprve po objevení se druhé ataky mluvíme o klinicky definitivní RS. Již v období CIS ale můžeme s určitou pravděpodobností předpovědět výskyt 2. ataky (Fisniku, Brex et al. 2008).
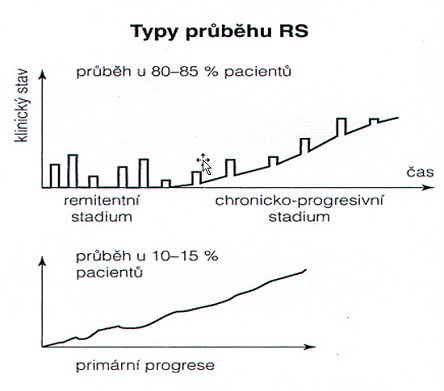
Pokud pacienta v úvodu nemoci nebudeme nijak léčit, tak nejpravděpodobnější prognóza je následující: během prvních 10–20 let se u pacienta budou střídat ataky a remise. Ataky mohou být buď stejné, nebo s různými příznaky, v období remisí by měl být stav stabilizovaný, i když může zůstat určité zbytkové postižení po předchozí atace. Jak časté budou ataky a intervaly mezi nimi, zatím bohužel předpovědět neumíme.
Průměrně po 15 letech od počátku nemoci se 60–80 % pacientů překlopí do tzv. sekundární progrese, tj období, kdy jsou ataky už málo časté a pacient se pozvolna zhoršuje. Důvodem tohoto zlomu je vyčerpání rezerv nervového systému. Nemoc je totiž zrádná v tom, že i v mezidobí remisí, kdy to vypadá, že se nic neděje, zánět u většiny neléčených pacientů postupuje a ukusuje z nervových drah. Naštěstí jsme se všichni narodili s určitým nadbytkem nervových vláken a nervový systém je schopný tyto ztráty určitou dobu kompenzovat. Při aktivním zánětu se ale tyto rezervy časem vyčerpají a pak už chybějící vlákna nelze ničím nahradit.
Méně častou variantou nemoci je tzv. primárně progresivní RS (10–15 %), kdy zcela chybí ataky a u pacienta postupně narůstají neurologické obtíže.
Jaké jsou možnosti léčby
Co dnes můžeme dělat, abychom chorobnému procesu zabránili?
Nemoc zatím neumíme vyléčit, tedy neumíme opravit špatně nastavené geny. Neumíme ani slepit potrhaná nervová vlákna v době, kdy už se vyčerpaly rezervy nervového systému. Co však už umíme, a to docela dobře, je ovlivnit probíhající zánět. Pokud se nám podaří zánět zpomalit, nebo dokonce zastavit, tak je velká šance, že buňky imunitního systému nebudou ničit nervové buňky a to umožní normální fungování nervového systému.
Čím dříve se o zastavení zánětu pokusíme, tím lépe, protože samozřejmě na počátku nemoci je nervový systém v nejlepším stavu a máme tedy největší šanci mu pomoci (viz obr. 2). To je odpověď na otázku, proč je dnes maximální snaha diagnostikovat a léčit nemoc včas a proč ji u většiny pacientů musíme léčit trvale. Našimi léky totiž ještě neumíme odstranit příčinu, pouze řešíme následek, tedy chybnou a nadměrnou činnost imunitního systému a to bohužel musíme dělat celý život (Horáková 2008).
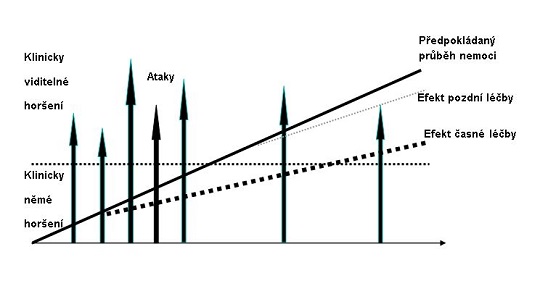
Velkou otázkou je, jak správně vybrat lék pro konkrétního pacienta a jak vyhodnotit, že lék funguje (Rio, Comabella et al. 2009). Ze studií, které sledovaly přirozený průběh nemoci v minulých letech, jistě víme, že pokud je nemoc neléčena, vede u většiny pacientů během 10–20 let k závažné invaliditě. Zároveň z jiných, vědecky podložených studií víme, že protizánětlivé léky mohou tento průběh podstatně ovlivnit. Neznamená to ale, že každý lék musí 100 % fungovat u každého pacienta. Jedinou možností, kterou tedy v současnosti máme, je začít s léčbou prakticky u všech rizikových pacientů a ty pak velmi pečlivě sledovat.
Cílem je, aby byl pacient bez atak, bez neurologického zhoršování a měl stabilní nález na rezonanci.
Pokud jsou všechny tyto parametry v normě, pak samozřejmě léčíme nejméně agresivními léky, dokonce v určitých případech zvažujeme i přerušení léčby s dalším pečlivým sledováním pacienta. Naopak pokud jsou jasné známky aktivity choroby (nové ataky, nová ložiska na MR a klinické horšení), tak se snažíme léčbu zesílit či změnit. Naštěstí se v současnosti naše možnosti výrazně zlepšují díky novým lékům, které jsou již registrovány nebo jsou ve fázích klinického zkoušení blízko před registrací.
Jak může pacient sám ovlivnit průběh choroby
Na rozdíl od celé řady tzv. civilizačních nemocí souvisejících např. s obezitou a kouřením, v případě roztroušené sklerózy zatím neznáme žádnou účinnou prevenci. Snad jedině pravidelný příjem vitaminu D a řádné vyležení probíhajících infekcí zejména v dětství představuje určitou prevenci. Nemocní roztroušenou sklerózou a také jejich potomci by rozhodně neměli kouřit, protože kouření je velmi pravděpodobně jeden ze spouštěcích faktorů.
Přesto ale pacient sám něco udělat může. Imunitní systém je velmi úzce provázán s nervovým systémem a psychikou a to, že tělo samo má nepochybně velké hojivé schopnosti, je známo odnepaměti. Je tedy velmi pravděpodobně, že pokud je člověk dobře naladěný s pozitivním přístupem k životu, tak lze očekávat i pozitivní signály z mozku do IS, které mohou pomoci zánětlivý proces ovlivnit.
Člověk se také musí pravidelně o své tělo starat. Není to totiž něco, co mu bylo dáno a během života by ho měl pouze devastovat. Obecně platí zásady zdravé výživy, jíst spíše méně, vyloučit co nejvíce všechny umělé látky a cukry, přijímat dostatek tekutin. Vitaminy je vhodné přijímat především v přirozené formě, nadměrné množství umělých vitaminů stejně není tělo schopné spotřebovat.
Nesmírně důležité je pravidelné cvičení. Je logické, že podstatně lépe vám budou sloužit svaly, které jsou pevné, zvyklé na určitou zátěž, než rozteklé a ochablé tělo. Navíc při pravidelném pohybu se v těle uvolňují tzv. vnitřní opiáty, endorfiny, které zlepšují náladu a mohou podstatně ovlivnit i bolest. Pokud pacient nemá žádné neurologické postižení, tak může cvičit bez omezení, tedy optimálně to, co ho baví a co zvládá, důležitá je zejména pravidelnost. V případě neurologického nálezu je třeba již speciální cvičení za pomoci zkušeného fyzioterapeuta, který pomůže vytvořit správný cvičební plán.
Roztroušená skleróza a těhotenství
Mezi časté dotazy jistě patří otázka RS a těhotenství (Horáková 2007). Dávno je již opuštěný názor, že by žena s roztroušenou sklerózou nemohla mít děti. Obecně platí, že u většiny pacientek, které jsou ve stabilizovaném stavu, není proti první graviditě žádných námitek. Těhotenství by mělo být plánované, je nutné předem anebo nejpozději v době zjištěné gravidity vysadit některé léky.
Vlastní těhotenství většinou vede ke stabilizaci nemoci. Rizikové je období prvních 6 měsíců po porodu, kdy se zvyšuje riziko ataky. Neznamená to ovšem, že by každá žena po porodu musela ataku dostat. Porod většina pacientek zvládne dobře, lze rodit všemi způsoby, tedy přirozeně i císařským řezem, tuto variantu ale nijak nepreferujeme, pouze pokud je gynekologický důvod. Lze užít i epidurální anestézii. Kojení doporučujeme 2–3 měsíce, pak postupně ukončit a vrátit se k původní medikaci. Pokud by se ale stav pacientky v závěru těhotenství zhoršil, zastavujeme kojení hned v úvodu.
Rozhodnutí o druhém a dalším těhotenství je vždy složitější, je nutno vzít do úvahy celkovou zátěž, kterou péče o potomky přináší. Pokud je pacientka stabilizovaná a má dobré zázemí, pak není námitek.
Roztroušená skleróza a dědičnost
Dalším častým dotazem je riziko dědičnosti. Většina epidemiologických studií ukazuje, že u přímých příbuzných pacienta s RS (rodiče, sourozenci, děti) je skutečně lehce zvýšené riziko výskytu RS. Zatímco v běžné populaci je výskyt RS asi 1–2 pacienti na 1000 obyvatel, tak u přímých příbuzných je to 20–30 pacientů na 1000 obyvatel, tedy pokud vezmeme 100 pacientů s RS, tak u 2–3 z nich bude mít někdo v rodině RS. Toto riziko je stále velmi malé a rozhodně nezakládá důvod k tomu, abychom naše pacienty nějakým způsobem omezovali. Důležité je také zdůraznit, že nemoc není v žádném případě nijak nakažlivá.
Očkování při roztroušené skleróze
Každé očkování představuje určitou stimulaci imunitního systému, a tedy jisté riziko aktivace relapsu a základního onemocnění. Výši tohoto rizika neumíme přesně určit. Samozřejmě to neznamená, že bychom se stavěli plošně proti všem očkováním. U onemocnění, kde očkování představuje jedinou rozumnou prevenci, např. běžná očkování v dětství nebo tetanus v dospělosti, proti očkování nemáme námitek.
Jiná situace je u výběrových očkování – např. klíšťová encephalitida, chřipka, hepatitida B v dospělosti, očkování před cestami do exotických krajin. Tady je třeba vždy vážit risk versus benefit, tedy zda je toto pro pacienta nezbytně nutné a zda se má zbytečně vystavovat riziku aktivace nemoci. Pokud se pacient pro tato výběrová očkování rozhodne, je zapotřebí očkovat vždy v době plné klinické stabilizace, mimo ataku, mimo infekci, po očkování je vhodný několikadenní relativní klidový režim. Ze zkušenosti lze říci, že pacienti tato očkování většinou zvládnou dobře. V případě imunosupresivní terapie nebo jiné biologické léčby, která výrazněji kompromituje imunitní systém, doporučujeme neočkovat živými vakcínami.
Omezení pacienta s roztroušenou sklerózou
Roztroušená skleróza je onemocnění celoživotní a pacient se s ním musí naučit žít. Lékař a ostatní zdravotničtí odborníci jsou zde proto, aby se za pomoci současných vědeckých poznatků maximálně snažili ovlivnit probíhající zánět a ulevit od případných negativních příznaků nemoci. Pokud se podaří stav stabilizovat (a to se nám naštěstí dnes již daří u řady pacientů), není důvod pacienta jakkoli omezovat. Naopak je maximální snaha o to, aby žil zcela normální život, včetně toho, aby pracoval, a tím alespoň částečně vrátil prostředky, které jsou vynakládány na ekonomicky velmi nákladnou léčbu.
V případě zhoršení klinického stavu, kdy pacient není schopen vykonávat plně svou původní profesi, jsou nesmírně důležité projekty umožňující zaměstnávání osob se sníženou pracovní schopností. Tedy vytvoření speciálně upravených pracovních podmínek, které umožní vyrovnat znevýhodnění způsobené nemocí. S tím souvisí i podpora všech projektů a aktivit, které zvyšují informovanost o nemoci samotné a problémech s ní spojených.
Závěr
Roztroušená skleróza je chronické, nelehké onemocnění, které bohužel umí předvést i dosti nepěknou tvář. Nemoc stále ještě neumíme vyléčit a pacient sám bez léčby není schopen provést žádnou známou prevenci, která by nemoc zastavila. Naštěstí věda a výzkum rychle postupují vpřed a posun v našich léčebných možnostech je za posledních 10 let opravdu výrazný. Všechny léky, které ovlivňují podstatu nemoci, ale fungují hlavně na začátku, tedy je třeba pacienty začít léčit co nejdříve. Rozsáhlý výzkum, který nadále probíhá, dává velkou naději do budoucna.
Člověk s RS nepotřebuje litovat, člověk s RS potřebuje být správně informován, potřebuje mít rychlý přístup k moderní léčbě a potřebuje pomoc při vytváření rovných podmínek, které mu umožní vyrovnat případný handicap způsobený nemocí.
doc. MUDr. Dana Horáková, PhD
Centrum pro demyelinizační onemocnění, Neurologická klinika 1. LF UK a VFN Praha
Literatura
FISNIKU, L. K., BREX, P. A. et al. (2008) Disability and T2 MRI lesions: a 20-year follow-up of patients with relapse onset of multiple sclerosis. In Brain, Vol. 131, Pt 3, pp 808–17.
HORÁKOVÁ, D. (2007) Roztroušená skleroza a mateřství. In Neurologie pro praxi, Vol. 1, pp. 32–34.
HORÁKOVÁ, D. (2008) Roztroušená skleróza a úloha praktického lékaře. In Medicína pro praxi, Vol. 10, pp. 378–382.
MONTALBAN, X., TINTORE, M. et al. (2010) MRI criteria for MS in patients with clinically isolated syndromes. In Neurology, Vol. 74, No. 5, pp. 427–34.
OKSENBERG, J. R., BARANZINI, E. et al. (2008) The genetics of multiple sclerosis: SNPs to pathways to pathogenesis. In Nat Rev Genet, Vol. 9, No. 7, pp. 516–26.
RAMAGOPALAN, S. V., MAUGERI, J. et al. (2009) Expression of the multiple sclerosis-associated MHC class II Allele HLA-DRB1*1501 is regulated by vitamin D. In PLoS Genet, Vol. 5, No.2, e1000369.
RIO, J., COMABELLA, M. et al. (2009) Predicting responders to therapies for multiple sclerosis. In Nat Rev Neurol, Vol. 5, No. 10, pp. 553–60.
WEINER, H. L. (2009) The challenge of multiple sclerosis: how do we cure a chronic heterogeneous disease? In Ann Neurol, Vol. 65, No. 3, pp. 239–48.

